グループ紹介
認知症グループ
研究テーマ
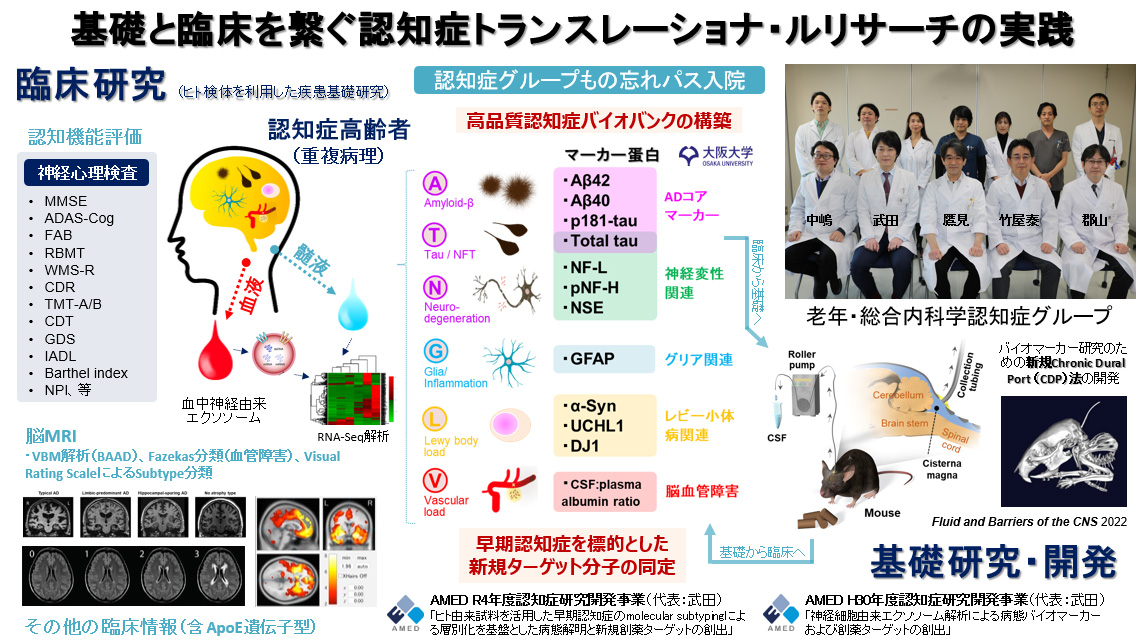
● 基礎と臨床を繋ぐ認知症トランスレーショナル・リサーチの実践
当グループでは、革新的なアプローチで認知症問題の克服を目指す幅広い研究を展開しています。認知症問題の根本的な解決のためには、アルツハイマー病の分子病態の解明や創薬といった基礎的な研究から、バイオマーカーの開発などの臨床研究、さらには認知症看護・介護領域における様々な現実的課題に対する実地研究まで、非常に幅広いアプローチが必要となります。当グループでは、認知症患者さんや家族・介護者の方の負担を少しでも軽減することを目指し、認知症診療や介護・看護の現場で起きていることを注意深く観察することで現状の課題点を明確にし、課題ドリブン型の研究開発を推進しています。
認知症という病気の全体を捉えて、包括的にアプローチするためには、医師や研究者に限らず幅広いバックグラウンドを持ったメンバーが一致団結して認知症研究に取り組むことが必要です。当グループでは、医師の他にも看護師、理学療法士、公認心理士、医学生、看護学生など、多職種のメンバーが互いに協力して日々研究に励んでいます。認知症の基礎研究や臨床研究、看護、介護に興味があり、自由な発想のもとに新しいソリューションを生み出す認知症研究に取り組みたい方は、是非お気軽にご連絡下さい。
連絡先: 武田朱公 takeda@cgt.med.osaka-u.ac.jp

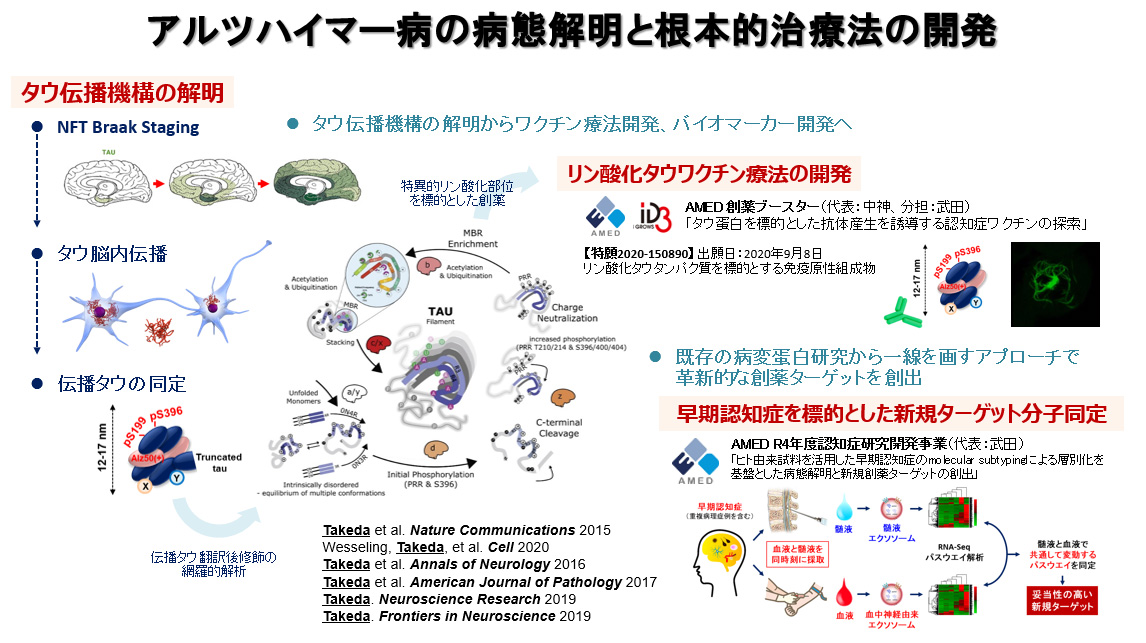
● アルツハイマー病の病態解明と根本的治療法の開発
認知症の原因疾患で最も多いのがアルツハイマー病であり、その根本的治療法の開発が望まれています。私たちのグループでは、アルツハイマー病の脳内に蓄積し神経細胞障害を引き起こす原因物質の一つと考えられているタウ蛋白に着目した基礎研究に取り組んでいます。
アルツハイマー病の脳内では過剰にリン酸化されたタウの凝集体が特定の脳領域に沿って出現することが知られており、この進展様式を説明する新しい病態仮説として「タウ伝播仮説」が提唱されています。タウ伝播仮説に関する研究はこの10年程で急速に進み、様々な知見が報告されアルツハイマー病の治療法開発の重要なターゲットとみなされています(Takeda. Frontiers in Neuroscience 2019、Takeda. Neuroscience Research 2019)。
武田らは、アルツハイマー病患者の剖検脳からタウ伝播を介在するタウ分子種(高分子量リン酸化タウ)を同定してその生化学的な特徴を明らかにし、この伝播タウが疾患修飾薬やバイオマーカー開発の標的となり得ることを世界に先駆けて報告してきました(Nature Communications 2015、Cell 2020、Annals of Neurology 2016、Ame J Pathol. 2017、EMBO J 2015、J Neurochem. 2016他)。またこの知見をもとにして、ペプチドワクチンの技術を用いてタウ伝播を抑制するアルツハイマー病治療ワクチンの開発を行っています(AMED創薬ブースターに採択)。
【関連する主要文献】
- Shuko Takeda, et al. Nature Communications, 6:8490, 2015
- H. Wesseling, Shuko Takeda, J. A. Steen, at al. Cell (20)31393-3. 2020
- Shuko Takeda*, et al. Annals of Neurology 80(3):355-67, 2016
- Wegmann S, Takeda S, Hyman BT, et al. EMBO J. 34(24):3028-41. 2015
- Shuko Takeda*. Frontiers in Neuroscience 13, pp1274, 2019
- Shuko Takeda*. American journal of Pathology. 01.022. 2017
- 武田 朱公 「抗タウ抗体」アルツハイマー病治療の新たなストラテジー p117-121 (2022)
- 武田 朱公 「タウ伝播を標的とした治療法開発」 医学のあゆみ 273(1): 23-27 (2020)
- 武田 朱公 「アルツハイマー病のタウ病理と治療法開発」 老年期認知症研究会誌 22(15): 94-96 (2019)
- 武田 朱公 「タウ脳内進展過程を標的とする診断・治療法の開発」 Dementia Japan. 33(3): (2019)
- 武田 朱公、中嶋 恒男:「認知症バイオマーカーとしてのCSFタウ」 実験医学 35(12): 152-155 (2017)
- 武田 朱公 「タウ伝播仮説の可能性と限界について」実験医学 35(12): 210-215 (2017)
【関連する知的財産権】
- 発明の名称:「リン酸化タウタンパク質を標的とする免疫原性組成物」、出願番号:特願2020-150890、出願日:2020年年9月8日、出願人:国立大学法人大阪大学、発明者:中神啓徳、武田朱公、他
- Title: RARE PHOSPHORYLATED HIGH MOLECULAR WEIGHT (HMW) TAU SPECIES THAT ARE INVOLVED IN NEURONAL UPTAKE AND PROPAGATION AND APPLICATIONS THEREOF, U.S. Application No.: 62/222,845, Inventors: Shuko Takeda and Bradly T. Hyman (米国特許出願)
【関連する主要外部資金】
- 科研費 若手研究A(代表:武田)「タウ病理の脳内進展過程を標的とした認知症に対する新規診断・治療法の開発」 2017〜2021年度
- 科研費 基盤研究B(代表:武田)「タウ病理の脳内進展過程を標的とした認知症の層別化・個別化治療に向けた基盤的研究」 2021年度〜
- 科研費 基盤研究B(分担:武田)「認知症関連病的蛋白の翻訳後修飾を標的としたワクチン療法の開発」 2022年度〜
- AMED 創薬ブースター(分担:武田)「タウ蛋白を標的とした抗体産生を誘導する認知症ワクチンの探索」2017〜2018年度
● 疾患基礎研究による認知症の新たな創薬ターゲットの創出
従来、アルツハイマー病の研究はAβやタウなどの病的蛋白の解析を主な対象として進められてきました。その成果の一部はAβ抗体療法のように実際の臨床応用に近づいていますが、認知症の克服にはまだ十分とはいえない状況です。また、従来の動物モデルや細胞実験を中心とした研究では、実際の認知症患者の脳内で生じている生物学的変化を捉えることが難しいことも分かってきています。未だに明らかになっていないアルツハイマー病の病態を解明し、真に有効な治療法の開発を行うためには、従来の病態仮説や研究手法に依存しない全く新しいアプローチが必要と考えられます。
当グループでは、早期の認知症患者を主な対象とした“疾患基礎研究”を実践することで、実際のヒト認知症患者の脳内で発症前後に生じている病態を解明することを目指しています。老年・総合内科学認知症グループとの連携のもと、高品質の生体サンプルを正確な臨床情報とともに収集し、高感度のトランスクリプトーム解析(RNA-Seq)や最新のバイオインフォマティクス技術を駆使した解析を行うことで、全く新しい認知症の病態仮説を導きそれを創薬に繋げる研究を推進しています。
【関連する主要外部資金】
- AMED R4年度 認知症研究開発事業 (代表:武田) 「ヒト由来試料を活用した早期認知症のmolecular subtypingによる層別化を基盤とした病態解明と新規創薬ターゲットの創出」 2022年度〜
- AMED 平成30年度 認知症研究開発事業 (代表:武田) 「神経細胞由来エクソソーム解析による病態バイオマーカーおよび創薬ターゲットの創出」 2018〜2021年度
● 認知症デジタルバイオマーカーの開発
近年、デジタル技術やAI解析を駆使した全く新しい認知症診断法の開発が国内外で進められています。当グループでは、アイトラッキング技術や画像AI解析を用いた認知機能評価法やフレイル評価法の開発とその社会実装に取り組んでいます。
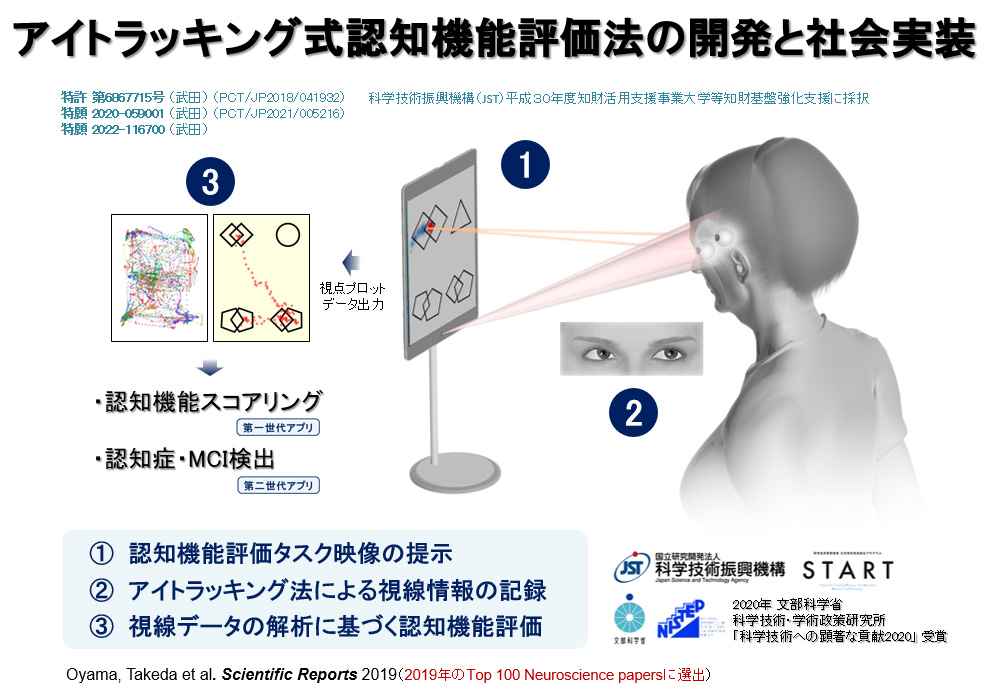
認知症の早期発見を困難にする要因として、従来の問診式認知機能検査に伴う被検者の心理的ストレスや、検査者側の人的労力・時間的負担の大きさが挙げられます。これらの課題を解決する手法として、当グループではアイトラッキング技術を利用した全く新しい認知機能評価法の開発とその実用化を進めてきました。
当グループが開発したアイトラッキング式認知機能評価法(Eye Tracking-based Cognitive Assessment:ETCA)は、約3分のタスク映像を眺める被検者の視線をアイトラッキング法で記録し、視線位置情報の解析から認知機能を定量評価するシステムで、従来の問診式認知機能検査のスコアと高い相関が得られることを実証してきました(Scientific Reports 2019)。さらにその汎用性の向上を目指し、画像AI解析によるアイトラッキング技術を利用することで、一般的なスマート・デバイスでも本検査法を実施できるソフトウエアを開発しました。これを基盤シーズとして大阪大学発ベンチャーのアイ・ブレインサイエンス社を設立し(JST大学発新産業創出プログラムSTARTにより支援)、本法の医療機器プログラムとしての開発を進めています。さらには、本法の言語依存性の低さと簡便性・汎用性を生かし、積極的な海外展開も進めています。世界中の認知症患者さんが少ない負担で認知機能検査を受けることができ、認知症の早期発見に繋がるシステムの構築と普及を目指しています。本研究成果は、2020年文部科学省・科学技術 学術政策研究所による「科学技術への顕著な貢献2020」に選出されました。
文部科学省・NISTEP Website: https://www.nistep.go.jp/archives/46302
YouTube動画: https://www.youtube.com/watch?v=rptyyx1tRaU
また、認知症と同様に高齢者医療における重要な課題とされているフレイルに対しても、デジタル技術を駆使した全く新しい評価法の開発を進めています。画像AI解析を用いたモーションセンサー技術を利用し、短時間で客観的に身体機能を評価することが出来るソフトウエアを開発しました。さらにこれを汎用スマート・デバイス上で利用するためのアプリを開発しています。従来、フレイルにおける身体機能の評価には専用の測定機器や広い測定場所を必要とし、被検者や検査者の負担が大きい点が課題として指摘されていましたが、本アプリではどこでも短時間で客観的な測定が可能になることが期待されます。
デジタル技術を駆使した全く新しい評価法やデジタルバイオマーカーの開発を進めることで、高齢患者さんの負担を軽減しながら、より正確な臨床的評価を行うためのプラットフォームを構築することを目指しています。
【関連する主要文献】
- Oyama, Takeda, et al. Scientific Reports 2019
(Scientific Reports誌のTop 100 Neuroscience papersに選出) - Katsuhisa, Takeda, et al. Dement Geriatr Cogn Disord. 2025
- “Eye-tracking app may speed up dementia diagnosis” Nature, Focal Point, Volume 612 Issue 7938, 2022
- 武田 朱公 医学と医療の最前線 「最近技術を用いた認知症の早期スクリーニング」、日本内科学会雑誌、2020年
- 武田 朱公 「アイトラッキングシステムを用いた認知症スクリーニングの可能性」、週刊医学界新聞(医学書院)、2020年
- 武田 朱公 「視線検出技術を利用した次世代型認知症検査法の開発」、BIOSCIENCE&INDUSTRY 2022年
- 武田 朱公 「加齢脳のバイオマーカー」、老年精神医学雑誌、2022年
【関連する知的財産権】
- 発明の名称:「認知機能障害診断装置および認知機能障害診断プログラム」、出願番号:特願2019-554215、特許第6867715号(PCT/JP2018/041932)、出願日:2018年11月13日、登録日:2021年4月13日、出願人:国立大学法人大阪大学、年発明者:武田朱公、他
⇒ 科学技術振興機構平成30年度知財活用支援事業大学等知財基盤強化支援に採択されPCT出願(PCT/JP2018/041932)。 - 発明の名称:「認知機能障害診断装置および認知機能障害診断プログラム」、出願番号:特願2020-059001、出願日:2020年3月27日、出願人:国立大学法人大阪大学、発明者:武田朱公、他
- 発明の名称:「ストループ検査方法、ストループ検査プログラム、ストループ検査システム、ストループ検査画像生成方法、ストループ検査画像生成プログラム、及び検査方法」、特願2022-116700、出願日:2022年7月21日、出願人:国立大学法人大阪大学、発明者:武田朱公、他
【関連する主要外部資金】
- JST-START 大学発新産業創出プログラム(代表:武田) 「視線検出技術を利用した簡易認知機能スクリーニングシステムの開発による社会システムの負荷軽減」 2018-2019年度
- 科研費 挑戦的研究萌芽(代表:武田) 「デジタルバイオマーカーとAIを基盤としたパーソナライズ型認知症予防プログラム開発」 2022年度〜
- 科研費 若手研究 (代表:大山、分担:武田) 「アイトラッキング式認知機能評価法の開発と認知症早期発見と介入に向けた実証研究」 2022年度〜
- 科研費 基盤研究B (代表:白井、分担:武田) 「ポジティブ心理健康資源と認知症発症の関連とメカニズム解明に関する観察・介入研究」 2022年度〜
- 科研費 基盤研究C (代表:中山、分担:武田) 「前立腺癌患者の高次脳機能に対する視線検出技術を用いた包括的機能評価」 2020年度〜
- 経済産業省ヘルスケアサービス社会実装支援事業(分担:武田) 「画像認識・対話AIを活用したフレイル・認知症予防プログラム」 2020年度
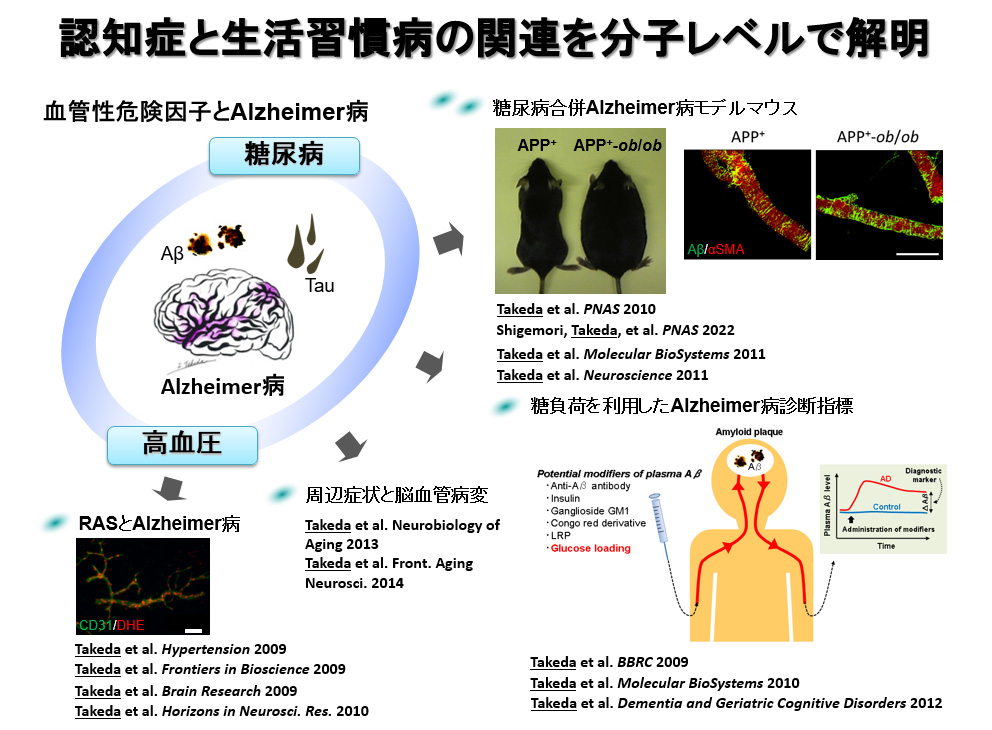
● 認知症と生活習慣病の病態連関の解明
近年の疫学研究から、糖尿病や高血圧などの生活習慣病が認知症の独立した危険因子であることが報告され、認知症予防のみならず新規創薬ターゲットの観点からも注目されています。
当グループでは、生活習慣病(糖尿病)とアルツハイマー病を合併する独自のモデルマウスを開発し、両疾患における相互的病態修飾機序を解明してきました(Takeda et al. PNAS 2010、Takeda et al. Molecular BioSystems 2011)。またこの中で、糖代謝が血中Aβ値に与える影響を明らかにし、この現象がアルツハイマー病の診断補助的指標として応用できる可能性を示してきました(Takeda et al. BBRC 2009、Takeda et al. Dement Geriatr Cogn Disord 2012、Takeda et al. Molecular BioSystems 2010)。またAβによる脳血管障害に着目し、高血圧における認知機能障害の病態解明(Takeda et al. Hypertension 2009)や、せん妄における脳血管障害の関与を明らかにしてきました(Takeda et al. Neurobiology of Aging 2013、Takeda et al. Front. Aging Neurosci 2014)。また最近では、血中Aβがインスリン分泌の生理的なモデュレーターとして膵臓に作用しているという画期的な知見を共同研究者とともに明らかにしました(Shigemori, Takeda, Tomiyama, et al. PNAS 2022)。
【関連する主要文献】
- Shuko Takeda, et al. Proc Natl Acad Sci U S A, 107(15), 2010
- Keiko Shigemori, Shuko Takeda, Takami Tomiyama, et al. Proc Natl Acad Sci U S A. 119(12), 2022
- Shuko Takeda, et al. Hypertension, 54(6), 2009
- Shuko Takeda, et al. Neurobiology of Aging 34(8), 2013
- Shuko Takeda, et al. Dement Geriatr Cogn Disord 9;34(1), 2012
- Shuko Takeda, et al. Biochemical and Biophysical Research Communications, 385, 2009
- Shuko Takeda, et al. Front. Aging Neurosci. 2014
- Shuko Takeda, et al. Molecular BioSystems, 7(6), pp1822-1827, 2011
- Shuko Takeda, et al. Molecular BioSystems, 6(10), pp1760-1766, 2010
- 武田 朱公: 「認知症の進行を規定する因子の解析と診断・治療法への応用」 Dementia Japan. (2021)
- 武田 朱公: 「レニン-アンジオテンシン系と認知症」日本臨牀 (2020)
- 武田 朱公, 楽木 宏実: 「高血圧制御と認知症予防」 Medical Science Digest. (2019)
- 武田 朱公: 「循環薬理学からみる認知症 生活習慣病・血管性危険因子と認知症の関連」 血管 (2019)
- 武田 朱公: 「血液脳関門の脆弱性とせん妄」 薬事日報. (2018)
- 大山 茜, 武田 朱公: 「認知症と高血圧」 Medical Practice. (2017)
- 武田 朱公: 「代謝性疾患と神経精神疾患を中心とした高次脳機能障害との関連 糖尿病とアルツハイマー病の相互的病態修飾関係」 日本神経精神薬理学雑誌. (2012)
- 武田 朱公, 里 直行, 森下 竜一: 「AT1受容体阻害薬による認知症病態修飾の新たな視点」 日本臨床. (2009)
- 武田 朱公, 里 直行, 荻原 俊男, 森下 竜一: 「高血圧とアルツハイマー型認知症」 血圧. 1 (2007)
- 武田 朱公, 中嶋 恒男, 森下 竜一: 「血管性認知症と生活習慣病の病態新展開」医学のあゆみ. (2017)
- 武田 朱公: 「脳血管病態の制御を基軸としたアルツハイマー病の革新的治療法の開発」 心臓. (2012)
- 武田 朱公, 里 直行, 森下 竜一: 「糖尿病合併症としてのアルツハイマー病」Cardiovascular frontier. 2(1): 17-22(2011)
- 武田 朱公, 里 直行, 楽木 宏実, 森下 竜一: 「糖尿病とアルツハイマー病における相互的な病態修飾機序の解明」 肥満研究 (2010)
【関連する知的財産権】
- 発明の名称:「アルツハイマー病の診断方法および診断薬」、特許第5704533号、登録日:2015年3月6日、出願人:国立大学法人大阪大学、発明者:武田 朱公、他
● モデル動物の脳内環境をリアルタイムで測定するための新規手法の開発
当グループでは、疾患モデルマウスを利用した基礎研究を促進するためのプラットフォームとして、覚醒自由行動下のマウス脳内タンパク質の変化をリアルタイムで評価するための手法の開発を進めてきました。従来、低分子量の神経伝達物質の回収などに利用されていたマイクロダイアリシス法を改良し、3000kDaという極めて大きな分子量の蛋白(あるいはその重合体)までを安定して回収することが出来る特殊な半透膜を有するプローブと還流システムの開発に成功しています(Takeda, et al. FASEB J 2013、Takeda, et al. Neurobiology of Aging 2013、Takeda, et al. Neuroscience 2011)。これにより、従来は困難とされていた生体マウス脳内からの認知症関連病的蛋白(Aβやタウ)の持続回収が可能になり、アルツハイマー病研究に応用されています(特許第4625914号)。またこの手法は既に製品化され、世界各国の研究室で利用されています。
https://www.eicom.co.jp/atmos
https://www.amuzainc.com/neuropeptide-microdialysis/
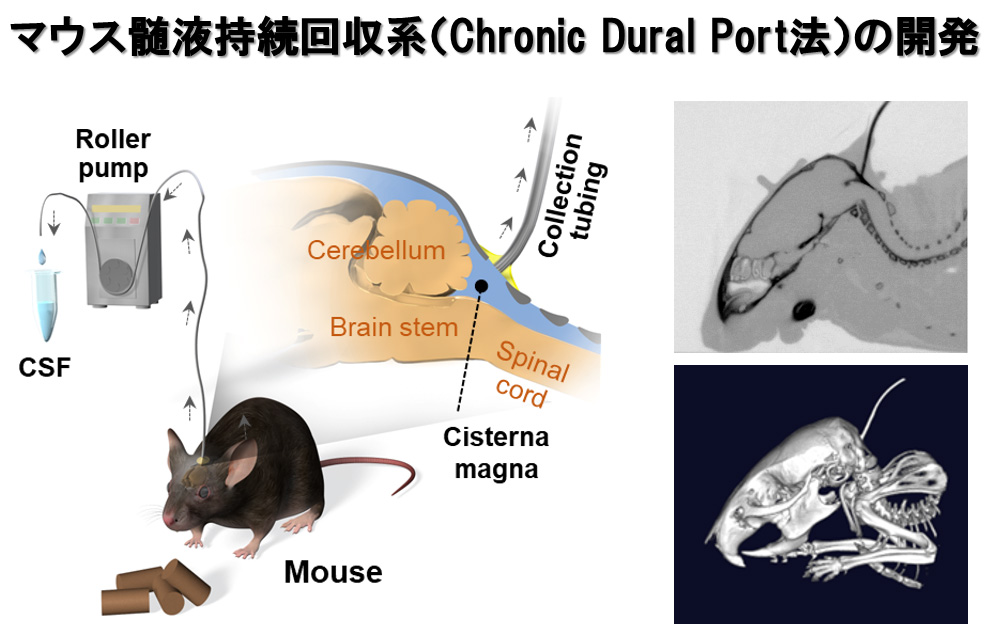
また最近では、覚醒自由行動下のマウスから脳脊髄液を持続的に回収することが可能な画期的なシステム(Chronic Dural Port(CDP)法)を開発しました(Nakajima, Takeda, et al. Fluids and Barriers of the CNS 2022)。従来の単回回収法では1個体のマウスから10μl程度の髄液しか回収することが出来ませんでしたが、CDP法では持続回収を行うことにより数十倍の容量の髄液回収が可能になりました。これにより、疾患モデルマウスを用いた髄液バイオマーカー解析が飛躍的に容易になることが期待されます。本手法をマニュアル化し(大阪大学発明届(N20180004))、アカデミアや大手製薬企業などへの技術指導も積極的に行っています。
【関連する主要文献】
- Shuko Takeda, et al. Neuroscience, 186, pp110-119, 2011
- Shuko Takeda, et al. Biochemical and Biophysical Research Communications, 385, pp193-197, 2009
- Shuko Takeda, et al. Neurobiology of Aging, 34(8), pp2064-70, 2013
- Shuko Takeda, et al. FASEB J, 27(8), pp3239-48, 2013
- Ksenia V., Shuko Takeda, Brian J. Bacskai, et al. Scientific Reports, 8964, 2019
- Arbel-Ornath M, Takeda S, Bacskai BJ. Et al. Mol Neurodegener. 12(1):27. 2017
- Muriel Arimon, Shuko Takeda, Oksana Berezovska, et al. Neurobiology of Disease. 84:109-19, 2015
- Hori Y, Takeda S, Hudry E. et al. J Biol Chem. 290(4):1966-78. 2015
- Hudry E, Takeda S, Hyman BT, et al. Sci Transl Med. 5(212) pp212-161, 2013
- Tadafumi Hashimoto, Shuko Takeda, Bradley T Hyman, et al. J Neurosci, 32(43):15181-92. 2012
【関連する知的財産権】
- 発明の名称:「新規マイクロダイアライシス回路を用いた脳内物質の精密測定方法」、特許第4625914号、登録日:2010年11月19日、出願人:国立大学法人大阪大学、発明者:武田朱公、他
- 発明の名称:「覚醒・自由行動下でのマウス脳脊髄液回収システム」、大阪大学発明届(N20180004)、届出日:2018年6月5日、発明者:武田朱公、中嶋恒男、他
[認知症グループ]